Accueil > > Santé > > Essieu de camion Marché Taille, tendances, perspectives, analyse régionale (2024-2031)
Marché des systèmes de gestion des données cliniques - taille, part, tendances de l'industrie et prévisions (2024 - 2031)
ID : CBI_1533 | Mis à jour le : | Auteur : Yogesh K | Catégorie : Santé
Systèmes de gestion des données cliniques Taille du marché :
Systèmes de gestion des données cliniques La taille du marché augmente avec un TCAC de 13,6% au cours de la période de prévision (2024-2031), et le marché devrait être évalué à US$ 4 490,53 millions d'ici 2031, contre US$ 1 837,50 millions en 2023.
Systèmes de gestion des données cliniques Marché Portée et aperçu :
Les systèmes de gestion des données cliniques sont des plates-formes logicielles utilisées pour la collecte, la gestion et l'intégration des données des essais cliniques. Les systèmes CDM sont efficaces pour s'assurer que les données recueillies lors des essais cliniques sont exactes et conformes aux exigences réglementaires. Les MDP sont équipés pour collecter autant de données que possible disponibles aux fins d ' analyse et peuvent rationaliser la procédure de saisie, de validation et de stockage des données. Ils effectuent également des pistes de vérification en suivant tout changement apporté aux données données en tenant un registre détaillé des modifications et des approbations de données. Les systèmes du MDP présentent plusieurs avantages, mais le principal est la fourniture de données de qualité et sans erreur. Il accélère également le processus de collecte des données, ce qui le rend efficace en réduisant le temps tout en promettant le respect des réglementations mondiales et locales. Les systèmes du MDP sont rentables, évolutifs et offrent un accès en temps réel aux données. Les systèmes du MDP sont souvent utilisés par des entreprises pharmaceutiques, des organismes de recherche sous contrat, l'industrie médicale, des établissements universitaires, etc.
Dynamique du marché des systèmes de gestion des données cliniques - (ORD) :

Pilotes clés :
L'augmentation du volume des essais cliniques fait progresser le marché
Les essais cliniques génèrent de grandes quantités de données que les systèmes de gestion des données cliniques gèrent, stockent et analysent précisément et efficacement. Avec l'avènement d'un plus grand nombre d'entreprises pharmaceutiques, d'organismes de recherche et d'établissements médicaux qui mènent des essais cliniques pour mettre au point de nouveaux vaccins, médicaments et dispositifs, la nécessité de conserver et de gérer efficacement les données s'est accrue. Cela a rendu les essais cliniques plus complexes, avec des recherches multidisciplinaires et multi-sites axées sur la médecine curative qui respectent des exigences réglementaires strictes. Le passage à la saisie électronique des données (EDC) et à des solutions numériques dans le cadre d'essais cliniques a renforcé l'adoption de systèmes CDM avancés. Les systèmes avancés offrent un accès direct aux données avec moins d'erreurs et des délais d'essai plus rapides. L'intégration de l'intelligence artificielle (IA) transforme également l'efficacité des systèmes du MDP, ce qui stimule sa demande.
- En février 2023, L'Organisation mondiale de la santé (OMS) a publié un article soulignant le nombre croissant d'essais cliniques réalisée de 1999 à 2022. La forte concentration d'essais cliniques dans la région Asie-Pacifique (APAC) a augmenté ces dernières années. Alors que l'Amérique du Pacifique occidental connaît une hausse récente par rapport aux nations européennes ou du Moyen-Orient.
Ainsi, les essais cliniques décentralisés et centrés sur le patient conduisent à la croissance du marché des systèmes de gestion des données cliniques.
Restrictions clés :
La protection des données et les préoccupations de sécurité freinent la croissance du marché
Les données recueillies au cours des essais cliniques sont des renseignements sensibles au patient qui comprennent les dossiers de santé, les chronologies médicales et les renseignements génétiques. Toute violation ou utilisation abusive de ces informations peut avoir des conséquences éthiques, financières et juridiques importantes pour les entreprises qui mènent les procès. Les gouvernements et les organismes de réglementation imposent des lignes directrices strictes sur la façon dont les données recueillies doivent être stockées et partagées. Les systèmes du MDP qui ne respectent pas les normes sont susceptibles de devenir obsolètes et les entreprises sont accusées d'amendes lourdes. Il y a aussi la vulnérabilité d'être une cible pour les cyberattaques de pirates qui tentent de voler des données confidentielles de patients pour les manipuler ou voler pour leur propre profit. Cela conduit à une méfiance générale parmi les patients qui participent à des essais cliniques, ce qui entrave l'adoption généralisée du système CDM.
- Par exemple, en août 2021, Morley Compagnies a subi une attaque ransomware conduisant à une brèche dans ses systèmes. Cela leur a coûté des données sur plus de 521 000 personnes. Ces personnes ont été informées en février 2022.
Par conséquent, la croissance du marché des systèmes du MDP est considérablement réduite, car le risque de violation des données ou de non-respect de la confidentialité des données reste viable sur le marché.
Possibilités futures :
L'adoption croissante des CDMS basés sur le cloud ouvre de nouvelles avenues pour l'expansion du marché
Les systèmes CDM basés sur le cloud sont plus rentables à long terme que les systèmes sur site classiques car ils réduisent le besoin d'infrastructures informatiques, de matériel et de maintenance coûteuses. Cela permet aux entreprises fabriquant des systèmes au titre du MDP d ' allouer plus efficacement leurs ressources pour rendre ces systèmes plus accessibles. Cette évolutivité permet aux entreprises d'ajuster facilement leur capacité de stockage et de traitement des données en fonction de la taille et de la complexité des essais cliniques spécifiques. Les systèmes CDM basés sur le cloud offrent une meilleure collaboration entre les intervenants cliniques et fournissent les services à distance aux partenaires. Il soutient également des essais cliniques décentralisés au cours desquels des données sont recueillies auprès de patients en dehors des cadres conventionnels, ce qui rend le processus flexible. Il permet l'intégration de données provenant de sources variées, comme les tests de santé à domicile, offrant des solutions basées davantage sur le cloud.
- Fountain est une société de solutions logicielles et de données qui fournit à ses clients des systèmes de gestion de données cliniques basés sur le cloud. Ils possèdent une expertise exceptionnelle dans les services de conseil en médecine, santé, biotechnologie, pharmacologie, etc. Leurs Systèmes fondés sur le MDP simplifier les essais cliniques et respecter les lignes directrices de tout protocole. Leurs systèmes CDM sont efficaces pour tous les instruments, médicaments et études diagnostiques.
Ainsi, comme les systèmes CDM basés sur le cloud offrent une meilleure analyse des données, ils ouvrent de nouveaux débouchés sur le marché des systèmes de gestion des données cliniques.
Systèmes de gestion des données cliniques Analyse sectorielle du marché :
Par type:
Le marché est segmenté selon le type de logiciel d'entreprise sous licence, de logiciel Web et de logiciel Cloud.
Tendances du type :
- Récemment, la tendance à intégrer les systèmes du MDP à l'intelligence artificielle (IA) et à l'apprentissage automatique (ML) a augmenté. Il en résulterait le traitement de grandes quantités de données provenant de sources différentes.
- La preuve du monde réel (RWE) est une tendance et est utilisée pour rendre les décisions en matière de soins de santé plus appropriées à l'usage du monde réel en tenant compte d'une approche plus centrée sur le patient.
Les logiciels basés sur le cloud représentaient la part de marché la plus importante des systèmes de gestion des données cliniques et devraient connaître la croissance la plus rapide au cours de la période prévue.
- Les logiciels basés sur le cloud offrent aux organismes de soins de santé la possibilité d'évoluer facilement sans investissements initiaux dans des infrastructures supplémentaires.
- Avec l'expansion des essais cliniques dans la portée et la complexité, la flexibilité des logiciels basés sur le cloud assure des ajustements rapides pour englober des ensembles de données plus grands et de nouvelles exigences d'essai.
- Les logiciels basés sur le cloud sont rentables car ils éliminent le besoin de matériel sur site coûteux et offrent des modèles «pay-as- you-go».
- Ils ont un protocole de sécurité robuste qui comprend le chiffrement de bout en bout, l'accès basé sur le rôle, et les mises à jour fréquentes pour se conformer aux normes de soins de santé.
- Par exemple, en mars 2023, Fujitsu Limited a annoncé le lancement d'un nouveau logiciel cloud pour la collecte de données relatives à la santé. Cette nouvelle plateforme est conçue pour tirer parti de l'IA et a une conversion automatique des données qui vise à révolutionner le domaine médical.
- Ainsi, la dérive croissante des essais cliniques décentralisés a accéléré l'adoption du logiciel de système CDM basé sur le cloud, ce qui a stimulé les tendances du marché des systèmes de gestion des données cliniques.
Par composante :
Le marché est bifurqué sur la base de composants dans les logiciels et les services.
Tendances de la composante :
- Récemment, une tendance à tirer parti des blockchains pour la sécurité des données dans les services est apparue pour sa capacité à créer des dossiers de patients immuables et inviolables.
- Ces derniers temps, il y a eu une tendance à adapter le logiciel du système CDM pour soutenir les essais cliniques décentralisés (DCT) qui peuvent recueillir des données à partir de sites éloignés.
En 2023, les logiciels représentaient la plus grande part du marché des systèmes de gestion des données cliniques.
- L'apparition de maladies complexes et rares, le besoin de médicaments personnalisés a augmenté, ce qui nécessite des essais cliniques précis. Ces essais nécessitent l'utilisation de logiciels spécialisés qui permettent de suivre, d'analyser et de stocker les données des patients.
- Les solutions logicielles avancées offrent une gestion efficace de grands volumes de données cliniques. Ils offrent également des capacités d'automatisation, de rationalisation des processus d'essai.
- Ces logiciels augmentent l'efficacité et accélèrent les délais d'essai en éliminant l'effort manuel et l'erreur humaine, les rendant attrayants pour les entreprises pharmaceutiques, les installations médicales, etc.
- L'adoption de systèmes de saisie électronique des données (EDC), un type de logiciel du système CDM, pour remplacer les méthodes classiques dans les essais cliniques est en hausse. Ils sont plus fiables et présentent un risque moindre de perte de données, ce qui améliore la précision des données.
- Par exemple, OpenClinica est un logiciel ouvert de gestion des données cliniques qui est efficace dans la gestion des données des essais cliniques. Le logiciel est flexible et rentable.
- Par conséquent, les solutions logicielles offrent un plus grand degré de personnalisation et de flexibilité, ce qui stimule la croissance du marché des systèmes de gestion des données cliniques.
Les services devraient connaître la croissance la plus rapide du TCAC sur le marché des systèmes de gestion des données cliniques au cours de la période prévue.
- La tendance croissante à confier des tâches de gestion des données cliniques à des fournisseurs de services spécialisés aide les entreprises pharmaceutiques, les entreprises de biotechnologie, etc. à réduire les charges opérationnelles et à gérer les coûts.
- Les services offrent des connaissances curées pour s'assurer que les essais cliniques respectent les normes réglementaires internationales, notamment en matière d'intégrité, de sécurité et de rapports.
- Les essais cliniques exigent une personnalisation de la gestion des données en fonction de domaines thérapeutiques particuliers, d'études de recherche et de lieux. Les services offrent une vivacisation par la conception de protocole, la configuration de la base de données, etc.
- Par exemple, Quantité, une entreprise de biotechnologie, offre des services de systèmes de gestion de données cliniques de pointe. Ils ont des dispositifs de capture électronique (EDC), des solutions CDM de bout en bout et des données d'essais cliniques de qualité exceptionnelle.
- Ainsi, les services offrent une formation et un soutien technique rentables, ce qui stimule l'expansion du marché des systèmes de gestion des données cliniques.
Par mode de livraison:
Le marché est segmenté en fonction du mode de livraison en On-Premise, Cloud-Based et Web-Based.
Tendances du mode de prestation :
- Récemment, la croissance constante de la télémédecine sur le Web et de la surveillance à distance a conduit à la mise au point de systèmes intégrés au titre du MDP qui peuvent transformer plusieurs dispositifs de surveillance en une seule plateforme.
- Les solutions basées sur le cloud peuvent désormais soutenir l'interopérabilité, ce qui contribue à une bonne coordination et communication entre les différents systèmes du MDP.
La livraison en nuage représentait le chiffre d'affaires le plus important et devrait connaître la croissance la plus rapide au cours de la période prévue.
- La livraison en nuage offre des mesures de sécurité améliorées, comme le chiffrement, l'authentification des utilisateurs, les pistes d'audit, etc. Ceci est conforme aux exigences médicales et aux lignes directrices réglementaires.
- La livraison en nuage permet l'accès en temps réel aux données qui peuvent accélérer la prise de décisions, améliorer la surveillance des essais et minimiser les retards, ce qui permet d'obtenir des résultats et des durées d'essai efficaces.
- Ils permettent l'intégration d'analyses avancées pour améliorer l'efficacité des essais en prédisant les résultats, en identifiant les modèles, en optimisant les conceptions et en gérant des ensembles de données complexes.
- Par exemple, Roulette offre des services en nuage pour leurs systèmes de gestion des données cliniques. Leurs systèmes permettent de recueillir facilement et d'intégrer des données provenant de sources variées telles que les appareils portables, les dispositifs de DSE, les patients, etc.
- Ainsi, l'implantation et le déploiement rapides des systèmes de gestion des données en nuage stimulent la demande sur le marché des systèmes de gestion des données cliniques.
Par demande :
Le marché est segmenté en fonction de l'application en Pharmacovigilance, Gestion des données d'essais cliniques, Conformité réglementaire et Recherche médicale.
Tendances de l'application :
- Récemment, la gestion des données sur les essais cliniques a insisté sur une approche plus axée sur le patient et fondée sur la valeur pour obtenir plus d'efficacité dans la collecte des données analytiques.
- La recherche médicale a récemment tenu compte des répercussions de la surveillance de la santé mentale et de la gestion du stress sur l'obtention d'informations plus précises sur les patients au cours des essais.
L'analyse des essais cliniques a représenté la plus grande part des revenus du marché des systèmes de gestion des données cliniques en 2023.
- L'augmentation du nombre d'essais cliniques, en particulier pour l'oncologie ou les maladies rares, engendre une demande de systèmes efficaces de gestion des données des essais cliniques.
- Les données générées nécessitent des contrôles de gestion, d'analyse et de conformité en temps opportun que les systèmes de gestion des données des essais cliniques sont spécifiquement conçus pour offrir.
- Les données des essais cliniques sont souvent complexes et les systèmes de gestion des données des essais cliniques offrent des caractéristiques comme EDC, la surveillance en temps réel et l'analyse améliorée pour traiter les complexités.
- L'expansion des technologies biopharmaceutiques et médicales pour les thérapies géniques, les produits biologiques, etc., a rendu nécessaire la mise au point de modèles d'essai uniques pour répondre aux besoins réglementaires.
- Par exemple, Conseil offre un système de gestion des données d'essais cliniques qui gère efficacement tous les aspects des essais cliniques du démarrage au gros plan. Il aide à centraliser les données relatives aux codes, sujets, finances, facturation, etc.
- Ainsi, à mesure que l'importance des essais cliniques augmente à l'échelle mondiale, une analyse robuste des essais cliniques assure la cohérence des données, ce qui stimule la demande sur le marché des systèmes de gestion des données cliniques.
On s'attend à ce que la pharmacovigilance ait le TCAC qui connaît la croissance la plus rapide au cours de la période prévue.
- La pharmacovigilance est impérative pour la surveillance de l'innocuité et de l'efficacité des médicaments, depuis les essais cliniques jusqu'à l'inspection après la mise en marché. Avec la fréquence croissante des essais cliniques, la demande de systèmes précis de gestion des données de pharmacovigilance augmente.
- Pour se conformer aux règles strictes fixées par les autorités sanitaires mondiales, les entreprises pharmaceutiques doivent maintenir des normes élevées en matière de rapports de pharmacovigilance et de gestion des données. Ils s'appuient sur des systèmes CDM avancés dotés de modules de pharmacovigilance intégrés pour satisfaire aux normes.
- La demande croissante de médicaments personnalisés et de thérapies complexes a rendu l'emploi de systèmes de pharmacovigilance avancés plus nécessaire pour surveiller les effets à long terme.
- Les patients et les travailleurs de la santé sont maintenant proactifs dans la déclaration des événements indésirables au cours des essais cliniques, ce qui stimule la demande de systèmes de pharmacovigilance sûrs et efficaces.
- Ainsi, le nombre croissant d'approbations de médicaments et les préoccupations concernant l'innocuité des médicaments renforceraient les tendances du marché des systèmes de gestion des données cliniques.
Par utilisateur final :
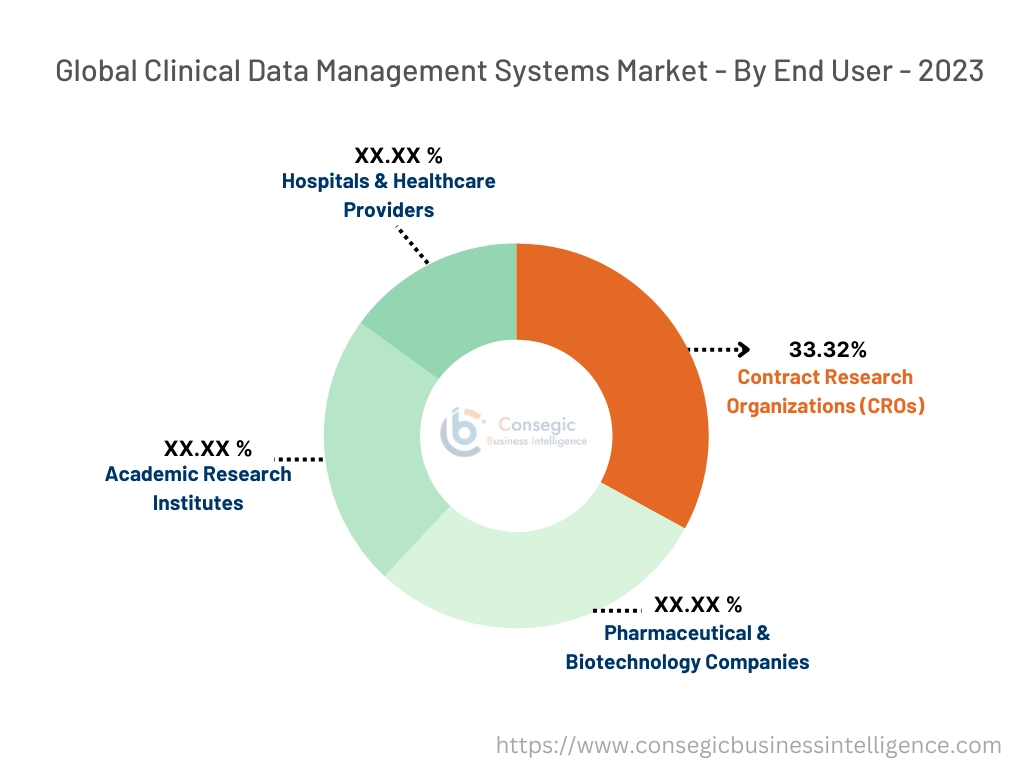
Le marché est segmenté en fonction des utilisateurs finals dans les sociétés pharmaceutiques et de biotechnologie, les organismes de recherche sous contrat (ORC), les instituts de recherche universitaires et les hôpitaux et fournisseurs de soins de santé.
Tendances de l'utilisateur final :
- Récemment, les entreprises de biotechnologie intègrent l'IA pour mettre au point de nouveaux médicaments à l'aide des données recueillies grâce aux systèmes avancés du MDP.
- La tendance à utiliser des modèles d'essais adaptatifs dans les hôpitaux et par les fournisseurs de soins de santé offre une approche plus innovante des essais cliniques.
En 2023, les organismes de recherche contractuels (ORC) représentaient la plus grande part des revenus, soit 33,32 %.
- Les organismes de recherche contractuels (ORC) deviennent une option fiable pour gérer la complexité des essais cliniques à mesure que l'externalisation des activités cliniques augmente.
- Les ORC sont des solutions de rechange rentables aux entreprises pharmaceutiques et de biotechnologie, car ils offrent des services spécialisés qui améliorent l'efficacité des essais cliniques en réduisant les erreurs pour la gestion des données cliniques.
- Les ORC sont souples pour adopter et intégrer des technologies de pointe telles que l'IA, l'apprentissage automatique et l'analyse améliorée dans leur processus de gestion du MDP.
- Ils offrent des essais cliniques décentralisés et hybrides en utilisant des systèmes CDM avancés capables de traiter à distance, de gérer les données en temps réel et de les intégrer.
- Par conséquent, les CRO offrent des services spécialisés comme l'analyse des biomarqueurs, les essais de médecine de précision et l'incorporation de données à partir des dossiers de santé numériques, ce qui stimule l'expansion du marché des systèmes de gestion des données cliniques.
Produits pharmaceutiques et biotechnologie Le TCAC devrait connaître la croissance la plus rapide au cours de la période prévue.
- L'accent mis sur les médicaments personnalisés a conduit les entreprises pharmaceutiques et de biotechnologie à mener des essais cliniques complexes et ciblés.
- Les essais cliniques nécessitent souvent la collecte et l'analyse de données génétiques et moléculaires que les systèmes CDM sophistiqués sont capables de traiter avec efficacité.
- L'expansion biologiques et biosimilaires dans le secteur pharmaceutique ont conduit à la production de plates-formes de systèmes CDM plus spécialisées qui peuvent gérer des données biologiques complexes.
- Les sociétés pharmaceutiques et de biotechnologie investissent activement dans la recherche et le développement (R-D) pour la mise au point de nouveaux traitements et thérapies, créant ainsi une adoption de systèmes CDM.
- Par exemple, Iqvia Inc. est une entreprise pharmaceutique, offrant une excellente gestion des données par des essais cliniques. Ils sont en mesure de développer de nouveaux traitements en analysant une solution stratégique axée sur les données.
- Ainsi, les systèmes du MDP sont importants pour les entreprises pharmaceutiques et de biotechnologie qui suivent et gèrent les données relatives aux événements indésirables, aux résultats déclarés par les patients, etc.
Analyse régionale :
Les régions concernées sont l'Amérique du Nord, l'Europe, l'Asie-Pacifique, le Moyen-Orient et l'Afrique, et l'Amérique latine.
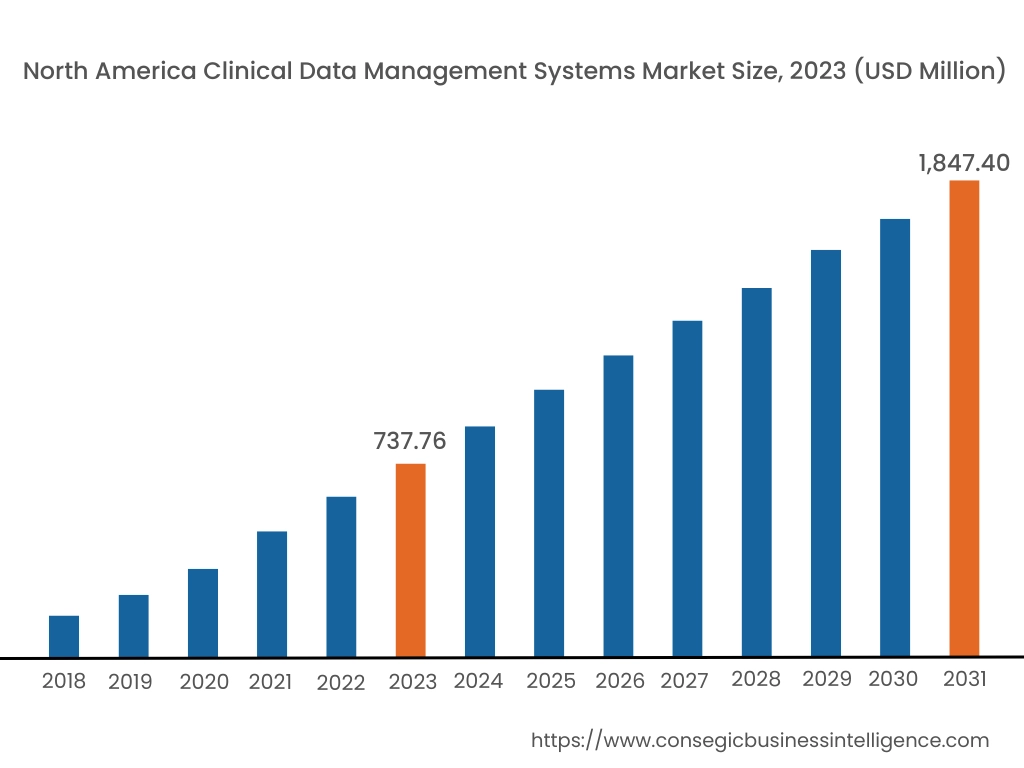
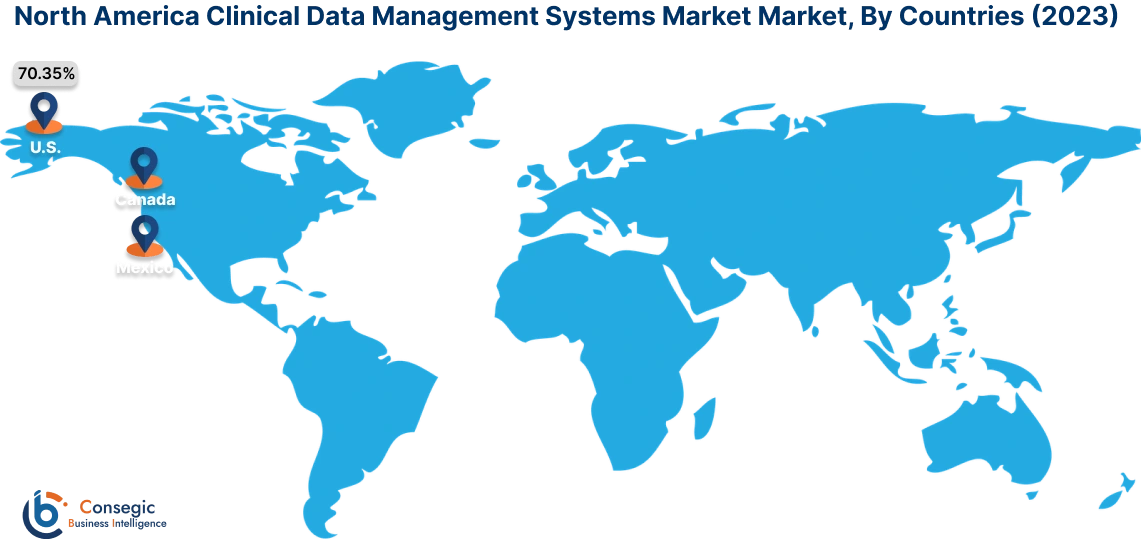
En 2023, l'Amérique du Nord représentait la part de marché la plus élevée (40,15%) et était évaluée à 737,76 millions de dollars et devrait atteindre 1 847,40 millions de dollars en 2031. En Amérique du Nord, les États-Unis ont représenté la part de marché la plus élevée (70,35%) au cours de l'année de référence de 2023. Selon l'analyse du marché des systèmes de gestion des données cliniques, en Amérique du Nord, en particulier aux États-Unis, le secteur des soins de santé et de la médecine possède l'infrastructure la plus avancée au monde. Le gouvernement s'inquiète activement de la sécurité et de l'intégrité des essais cliniques et applique des règles et des règlements stricts. Il en résulte des investissements accrus dans le développement de technologies de pointe pour des systèmes de gestion des données sophistiqués afin d'assurer la sécurité et la traçabilité des patients.
- Systèmes Veeva, une société de logiciels basée sur le cloud, dans un récent communiqué de presse (PR) traite des facteurs qui stimulent l'innovation en matière de données cliniques à New York.
L'Asie-Pacifique devrait connaître le TCAC le plus rapide au cours de la période de prévision de 14,6 % entre 2024 et 2031. Dans la région Asie-Pacifique (APAC), en particulier dans des pays comme la Chine, le Japon, l'Inde, la Corée du Sud, etc., les secteurs des produits pharmaceutiques et de la biotechnologie connaissent une expansion rapide. Cela a entraîné une augmentation du nombre d'essais cliniques menés dans cette région, grâce à l'investissement étranger et à la disponibilité d'une vaste base de patients. Il a rendu les CDM essentiels car ils gèrent et analysent de manière experte des données cliniques complexes.
- Un rapport publié par CMIC Exploitations, souligne la façon dont l'activité des essais cliniques a connu une expansion dans la région APAC. Le Japon, en particulier, est devenu un producteur de drogue de premier plan. Plusieurs autres pays de la région offrent des environnements propices à l'oncologie, aux maladies rares et à la thérapie cellulaire et génique.
Les marchés européens, en particulier au Royaume-Uni, en France, en Allemagne, etc., ont une adoption accrue de technologies de pointe comme l'informatique en nuage, les algorithmes d'intelligence artificielle (IA) et l'apprentissage automatique (ML) dans les essais cliniques. Les systèmes novateurs du MDP sont intégrés à ces technologies qui améliorent sa capacité à rationaliser l'analyse des données, le suivi des essais et le recrutement des patients.
L'analyse du marché des systèmes de gestion des données cliniques montre que la région du Moyen-Orient et de l'Afrique (MEA), en particulier la région du Golfe, se concentre sur la sécurité et la conformité des données. Cela les harmonise avec les contraintes réglementaires mondiales qui aident à intégrer leur secteur médical plus fermement dans l'ordre mondial.
En Amérique latine, le coût des essais cliniques est faible par rapport aux normes mondiales. Cela facilite l'externalisation des essais cliniques dans cette région par des entreprises pharmaceutiques, ce qui favorise l'adoption de systèmes de gestion des données pour gérer des opérations d'essai complexes et la confidentialité des données.
Principaux acteurs et parts de marché :
Le marché des systèmes de gestion des données cliniques est très concurrentiel avec les principaux acteurs fournissant des logiciels et des services aux marchés nationaux et internationaux. Les principaux intervenants adoptent plusieurs stratégies de recherche-développement (R-D), d'innovation dans les produits et de lancement des utilisateurs finaux pour occuper une position solide sur le marché mondial des systèmes de gestion des données cliniques. Les principaux acteurs de l'industrie des systèmes de gestion des données cliniques sont les suivants :
- Oracle (États-Unis)
- Médidonnées (États-Unis)
- Société IBM (États-Unis)
- Société internationale Parexel (États-Unis)
- Clario (États-Unis)
- Systèmes Veeva (États-Unis)
- DONNEES Société canadienne des postes (États-Unis)
- eClinical Solutions (USA)
- Santé des signataires (États-Unis)
- ICON plc (Irlande)
Développements récents de l'industrie :
Lancements de produits :
- En décembre 2023, Thermo Fisher Scientific a annoncé le lancement d'une plateforme de données en nuage, CorEvidence. Ce nouveau logiciel optimise le traitement des cas de pharmacovigilance et assure la sécurité des procédures de gestion des données cliniques. Il améliore les registres de recherche clinique CorEvitas offerts par l'entreprise de recherche clinique PPD. Il gère efficacement un large éventail de sources de données, rationalise le codage et signale des événements indésirables ainsi que des événements de sécurité pour les études de sécurité postautorisation.
- En février 2024, Revvity Signals a annoncé le lancement d'une unité logicielle et informatique qui peut rationaliser les données des essais cliniques. Le nouveau logiciel, Signals Clinical Solution, est une plateforme logicielle (SAAS) qui peut centraliser la gestion des données cliniques. Il est conçu pour accélérer d'importantes idées d'essais et des décisions fondées sur des données afin de révolutionner l'accès et l'analyse des données d'essais cliniques.
Fusions et acquisitions :
- En novembre 2023, Everest Clinical Research a dévoilé son intention d'acquérir la recherche d'août. Everest est un organisme de recherche sous contrat (ORC) qui possède une connaissance efficace de la gestion des données cliniques, de la biostatistique et de la programmation statistique. August Research est un organisme européen de recherche sous contrat (CRO) qui offre des services de services d'essais cliniques (CTS) et de pharmacovigilance (PV). Cette acquisition stratégique élargirait la portée mondiale d'Everest et établirait une tête de pont sur les marchés européens des essais cliniques.
- En avril 2024, GE Health a révélé l'achèvement de leur acquisition de logiciel MIM. GE Health est une entreprise innovante de diagnostics pharmaceutiques et de solutions numériques, alors que MIM Software est un fournisseur de solutions innovantes. Grâce à cette acquisition, GE Health gagne à intégrer les solutions d'analyse d'imagerie et de flux de travail numériques de MIM Software au portefeuille mondial de technologies médicales de GE. Elle renforcerait également la réponse de GE aux besoins des fournisseurs.
Partenariats et collaborations :
- En septembre 2024, l'Organisation européenne pour la recherche et le traitement du cancer (EORTC) a annoncé une prolongation de quatre ans du partenariat avec Medidata. Ce partenariat vise à faciliter l'accès des patients aux essais cliniques en oncologie en offrant une participation efficace aux essais. Il en résulterait la livraison de nouveaux traitements au marché à un rythme plus rapide. Grâce à cette collaboration, EORTC utiliserait 13 solutions Medidata qui offriraient à leurs chercheurs un accès complet et une gestion des données cliniques en un seul endroit.
Systèmes de gestion des données cliniques Rapport sur le marché Perspectives :
| Attributs du rapport | Détails du rapport |
| Échéancier de l'étude | 2018-2031 |
| Taille du marché en 2031 | 4 490,53 millions de dollars |
| TCAC (2024-2031) | 13,6% |
| Par type |
|
| Par composante |
|
| Par mode de livraison |
|
| Par utilisateur final |
|
| Par région |
|
| Acteurs clés |
|
| Amérique du Nord | États-Unis Canada Mexique |
| Europe | Royaume-Uni Allemagne France Espagne Italie Russie Benelux Reste de l'Europe |
| APAC | Chine Corée du Sud Japon Inde Australie ASEAN Reste de l'Asie-Pacifique |
| Moyen-Orient et Afrique | GCC Turquie Afrique du Sud Reste du MEA |
| LATAM | Brésil Argentine Chili Reste du LATAM |
| Couverture du rapport |
|
Questions Clés Répondues dans le Rapport
Quels sont les principaux acteurs du marché des systèmes de gestion des données cliniques ? +
Les principaux acteurs du marché sont Oracle (États-Unis), Medidata (États-Unis), IBM Corporation (États-Unis), Parexel International Corporation (États-Unis), Veeva Systems (États-Unis), Clario (États-Unis), DATATRAK International, Inc. (États-Unis), eClinical Solutions (États-Unis), Signant Health (États-Unis) et ICON plc (Irlande).
Quels détails de segmentation spécifiques sont couverts dans le rapport sur le marché des systèmes de gestion des données cliniques ? +
Le marché des systèmes de gestion des données cliniques est segmenté en type, technologie, mode de livraison, application et secteur d'activité de l'utilisateur final.
Quelle est la région qui connaît la croissance la plus rapide sur le marché des systèmes de gestion des données cliniques ? +
L’Asie-Pacifique est la région qui connaît la croissance la plus rapide sur le marché des systèmes de gestion des données cliniques.
